Alles über Gasmessgeräte
Erfahren Sie alles Wichtige rund um Gassmessgeräte und deren Funktionsweise.
Warum braucht man überhaupt Gasmessgeräte?
Im Laufe der Evolution hat sich der Mensch an die Erdatmosphäre angepasst. Der menschliche Organismus funktioniert optimal in grob gesagt 21 % Sauerstoff und 79 % Stickstoff. Dabei sind ubiquitär vorkommende Spurengase wie z. B. CO2 und Edelgase vernachlässigt. Kleine Abweichungen in der Zusammensetzung beeinträchtigen das Wohlbefinden, größere die Gesundheit und sehr große können tödlich sein. Toxische Gase können auch schon in sehr geringen Konzentrationen äußerst gesundheitsschädlich sein. Dabei unterscheidet man folgende Gefährdungen:
- Sauerstoffmangel
- Präsenz explosiver Gase
- Präsenz toxischer Gase
Die oben genannten Abweichungen können sowohl in der Natur auftreten, als auch durch den Menschen verursacht sein. In unserer industriellen Gesellschaft überwiegt letzteres. Typische Beispiele für natürliche Abweichungen sind Rotteprozesse, bei denen sowohl brennbare Gase (Methan) als auch toxische Gase (Schwefelwasserstoff, Kohlendioxid, Mercaptane u. v. m.) entstehen. Diese Gase reichern sich gerne in Gruben oder Senken an. Ein typischer Unfall ist der sogenannte Jauchegrubenunfall: Jemand kommt einer Jauchegrube zu nahe, inhaliert Schwefelwasserstoff, dieser führt zu einer Atemlähmung. Der Verunfallte fällt in die Grube und ertrinkt oder erstickt. Personen die versuchen ihm zu Hilfe kommen wollen ereilt das gleiche Schicksal.
Trotzdem ist es in landwirtschaftlichen Betrieben nicht üblich Gaswarngeräte mitzuführen. Ganz anders in abwassertechnischen Betrieben. In deren Becken finden ähnliche Faulprozesse statt. Schon der Zulauf im Bereich der Rechen wird mit stationärer Messtechnik auf brennbare Gase überwacht. Das eintreffende Abwasser könnte ja bereits Methan emittieren oder Treibstoffe bzw. Lösemittel mitführen. In den Arbeitsbereichen sind die Mitarbeiter mit Geräten ausgestattet, die sogar mehrere Gase detektieren können. Typischerweise messen diese brennbare Gase, Sauerstoffmangel, Kohlendioxid und Schwefelwasserstoff.
1. Ein Ausflug in die Geschichte
Dass bei der alkoholischen Gärung gefährliche Gase entstehen ist seit Antike bekannt. Seit Menschengedenken stellen Winzer eine Kerze auf den Boden ihrer Gärkeller, bei deren Verlöschen durch Sauerstoffmangel oder CO2 – Präsenz sie den Keller verlassen müssen. Natürlich konnten sie früher nicht wissen, dass die Gefahr durch Kohlendioxid entstand. Genauso wenig wussten sie, dass das Kohlendioxid bereits ab 0,5 % toxisch wirkt, die Kerze aber erst bei ca. 10 % erlischt.
Ein weiteres typisches Beispiel für natürlich vorkommende Gase ist der Bergbau. Die so genannten „schlagenden Wetter“ enthalten giftiges Kohlenmonoxid und explosives Methan. Daher ist es nicht verwunderlich, dass gerade im Bergbau sehr früh versucht wurde, die Gefahr durch Gas rechtzeitig zu erkennen. Schon bald nach Christi Geburt wusste man um die Gesundheitsgefahr beim Abbau von z. B. Quecksilber. In einer Schrift Plinius des Älteren ca. 100 n. C. wird dies beschrieben. Vergeblich versuchte man sich mit Masken aus Farn zu schützen.
Auch spätere Autoren (1556 Georgius Agricola: „De Re Metallica“, um 1700 und Bernardino Ramazzini: „De Morbis Artificium Diatribe“) wussten um die Gefahren durch Gas im Bergbau. Eine Möglichkeit das Gas nachzuweisen ist allerdings nicht überliefert. Da man damals noch gar nicht wusste, was ein Gas überhaupt ist, wäre dies auch schwer möglich gewesen. Daher liegt der Schluss nahe, dass es keine Möglichkeit gab zu beurteilen ob die Atmosphäre gefährlich war.
Als die industrielle Revolution die Förderung von immer mehr Kohle verlangte, stieg der Bedarf nach einer Messung gefährlicher Gase. Wohl gemerkt: Man wusste nicht, welche Substanzen die Gefahr auslösten, wohl aber wusste man um die Präsenz einer diffusen Gefahr.
Um eventuell gefährliche Gase zu beseitigen, schickte man Spezialisten, so genannte „Firemen“, voran. Brennbares Methan ist spezifisch leichter als Luft, reichert sich also unter der Decke an. Die Firemen hielten ein Kerze dicht unter die Decke, so dass diese dasMethan entzündete. Diese Methode war alles andere als ungefährlich. Hatte sich anstatt stark angereichertem Methan eine explosive Atmosphäre gebildet, konnte dies fatale Folgen haben. Fireman war ein sehr gefährlicher Beruf.

Gegen Mitte des 18. Jahrhunderts bemerkte man, dass gefährliche Substanzen das Erscheinungsbild einer Kerzenflamme verändern. Um die Kerze als Zündquelle unschädlich zu machen, versuchte man die Flamme durch Wassersäulen von der Atmosphäre zu trennen. Dieses Verfahren war aber sehr umständlich. Letztendlich setzte sich die Idee von Humphrey Davy durch, die Flamme durch engmaschige Metallnetze von der Atmosphäre abzutrennen. 1816 wurden in England die ersten Davy – Lampen erprobt. Dabei handelte es sich um Öllampen, deren Flamme hinter einer primitiven Art von Flammensperre brannte.
Für mehr als 150 Jahre sollte die Davy – Lampe im Original, und im Laufe der Zeit mit einigen Verbesserungen, die einzige Möglichkeit zur Gasdetektion sein. So gab es Versuche die Abschätzung der Flammenhöhe durch Anbringen einer Skala zu erleichtern. Die Installation eines Bimetall – Fühlers könnte man bereits als Vorläufer einer Flammentemperaturmessung bezeichnen. (Je mehr Methan vorhanden war, umso mehr Brennstoff stand zur Verfügung, umso heißer brannte die Flamme, umso stärker war die Auslenkung des Bimetalls.
Man hatte nun zwar ein Werkzeug mit dem man Licht erzeugen konnte, und mit dem man – mit einiger Erfahrung – die Präsenz gefährlicher Gase abschätzen konnte. Allerdings war dieses Verfahren darauf angewiesen, dass die Umgebungsluft genug Sauerstoff enthielt. Leider ist dies unter Tage keinesfalls sicher. Gott sei Dank haben sich seitdem die Methoden der Gasmesstechnik immer mehr verfeinert.
Also zurück in die Jetztzeit.
2. Wie funktionieren moderne Gaswarngeräte?
2.1 Messung brennbarer Gase
2.1.1 Katalytische Sensoren
Diese Sensoren machen sich die Eigenschaft brennbare Stoffe zunutze, bei ihrer Verbrennung Energie abzugeben. Deshalb nennt man sie auch Wärmetönungssensoren. Bei der Verbrennung von z. B. Methan passiert folgendes:
CH4 + 2 O2 -> CO2 + 2 H2O + Energie
Die bei dieser Reaktion abgegebene Energie ist umso größer, je mehr Methan in der Luft ist. Nun musste man sich nur noch eine Anordnung ausdenken, mit der man die abgegebene Energie genau bestimmen konnte. Dazu verwendet man zwei Keramikperlen (auch Pellistoren genannt), beide werden durch eine Platinwendel im Inneren auf ca. 400 °C aufgeheizt. Eine der Wendeln ist katalytisch beschichtet. An ihrer Oberfläche wird das Methan oxidiert, d. h. es wird Energie frei, die die Wendel weiter aufheizt. Diese Erwärmung erhöht den elektrischen Widerstand der Wendel. Die zweite Wendel ist nicht katalytisch beschichtet, an ihr findet keine Oxidation statt. Durch den Vergleich mit diesem passiven Element kompensiert man das Signal gegen äußere Temperaturschwankungen, Luftströmung, Feuchte etc. denn diese Einflüsse wirken auf beide Keramikperlen in gleicher Weise ein.
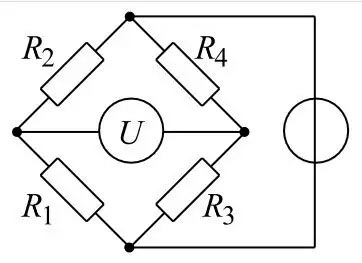
Eine sehr genaue Methode, Widerstandsänderungen zu messen, ist die Wheatstone `sche Brücke.
Man schaltet die zwei Wendeln als Äste einer Wheatstone `schen Brücke. Mit dieser Methode kann man die Widerstandsänderung sehr genau messen, und damit indirekt den Brennstoffgehalt der Atmosphäre. Dieses Signal kann man verwenden um zu beurteilen ob die Atmosphäre explosiv ist oder nicht. Dabei möchte man die tatsächliche Konzentration gar nicht wissen. Man möchte nur wissen, ob Explosionsgefahr droht oder nicht. Deshalb stellt man den Messbereich auf 0 – 100 % UEG ein (= Untere- Explosions- Grenze). Leider ist die UEG eine stoffspezifische Größe. Man muss also wissen, mit welchem Gas man es zu tun hat. Dann muss man in der Literatur nachschlagen, bei welcher Konzentration dieses Gases die UEG liegt.
Schwierig wird die Sache wenn Gasgemische auftreten können. Da man meist die anteilige Zusammensetzung nicht vorhersehen kann, hilft man sich mit einer sogenannten Sicherheitskalibrierung. Dabei stellt man sein Messgerät gar nicht auf das zu erwartende Gasgemisch ein, sondern auf eine Substanz, die mit weniger Empfindlichkeit detektiert wird. Gerne wird Nonan verwendet, da dieses eine sehr niedrige UEG besitzt. Da Nonan eine Flüssigkeit ist, wäre eine Kalibrierung auf Nonan im Feld allerdings sehr umständlich. Es ist schwierig und daher mit großem Fehler behaftet, im Feld eine genaue Gasmischung aus einer Flüssigkeit herzustellen.
Deshalb bietet Compur Monitors eine „Doppelkalibrierung“ an. Dabei wird im Labor mit Nonan kalibriert, und ein zweites Mal mit einem Referenzgas, z. B. Butan. Der Referenzfaktor wird auf dem Sensor vermerkt so dass der Anwender im Feld bequem mit einer Luft / Butan Mischung aus einer handelsüblichen Flasche kalibrieren kann. Auf diese wendet er dann den Referenzfaktor an.
Katalytische Sensoren haben viele Vorteile:
Natürlich gibt es auch Nachteile:
2.1.2 Infrarotsensoren
Viele Gase absorbieren Licht bei einer ganz bestimmten Wellenlänge. Jedes Molekül entnimmt einem Lichtstrahl eine bestimmte Anzahl von Lichtquanten. Diese Energie wird dazu verwendet, bestimmte Elektronen im Molekül in Schwingung zu versetzen. Glücklicherweise findet dieser Effekt nur bei ganz bestimmten Wellenlängen statt. Durch die richtige Auswahl der Wellenlänge kann man also bestimmen, welches Gas das Gerät messen soll. Zur Messung von Kohlenwasserstoffen wählt man 3,4 μ. Bei dieser Wellenlänge absorbiert die C – H Bindung der Kohlenwasserstoffe. Wenn man also die Menge der absorbierten Energie messen kann, kann man daraus auf die Menge der Gasmoleküle im Lichtweg schließen.
Ein Infrarot – Gasmessgerät ist also folgendermaßen aufgebaut: Man schickt einen Lichtstrahl durch eine Küvette and deren Ende sich ein Lichtdetektor befindet.
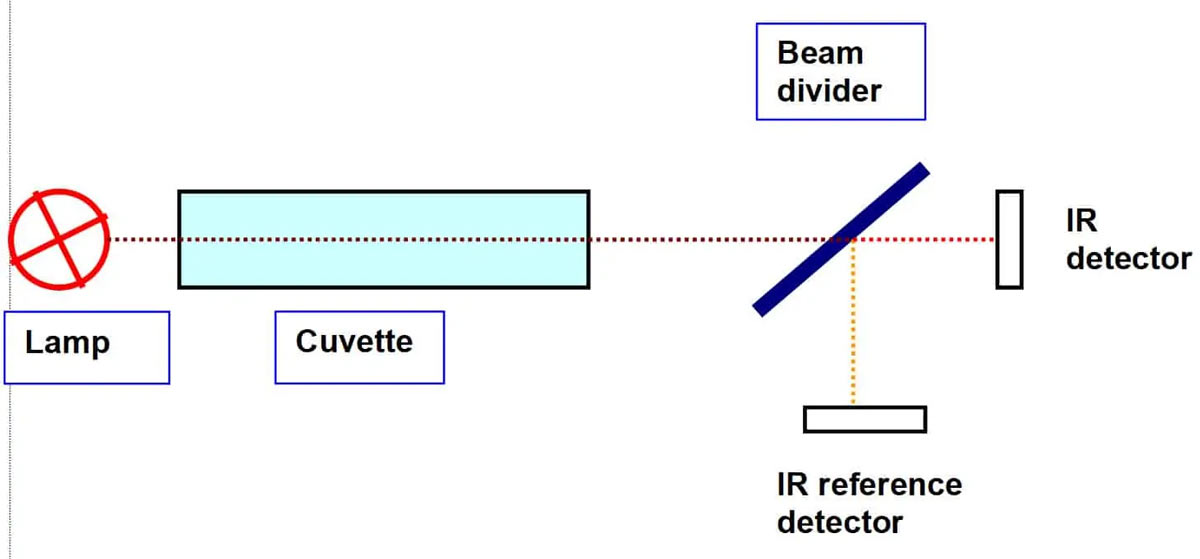
Je weniger Licht der Detektor empfängt, umso mehr Gas befindet sich in der Küvette. Um andere Umwelteinflüsse wie Feuchte, Druck oder Temperatur zu kompensieren verwendet man einen zweiten Strahl mit einer anderen Wellenlänge. Um Licht einer ganz bestimmten Wellenlänge zu erzeugen, verwendet man Filter, optische Gitter, Prismen oder gleich LED Lichtquellen einer bestimmten Farbe.
Genauso gut kann man einen einzigen Lichtstrahl hinter der Küvette in Zwei Strahlen unterschiedlicher Wellenlänge aufteilen.
Infrarotsensoren haben einige Vorteile:
Natürlich gibt es auch Nachteile:
2.1.3 Flammentemperatursensoren
Wie bei der Davy – Lampe schon beschrieben, erhöht die Anwesenheit eines brennbaren Gases die Temperatur einer Flamme. Meist verwendet man eine Wasserstoffflamme. Ein genauer Temperaturfühler in der Flamme kann die durch das Gas erzeugte Erhöhung der Temperatur einfach detektieren.
Flammentemperatursensoren haben einige Vorteile:
Natürlich gibt es auch Nachteile:
3. Messung toxischer Gase
3.1 Elektrochemische Sensoren
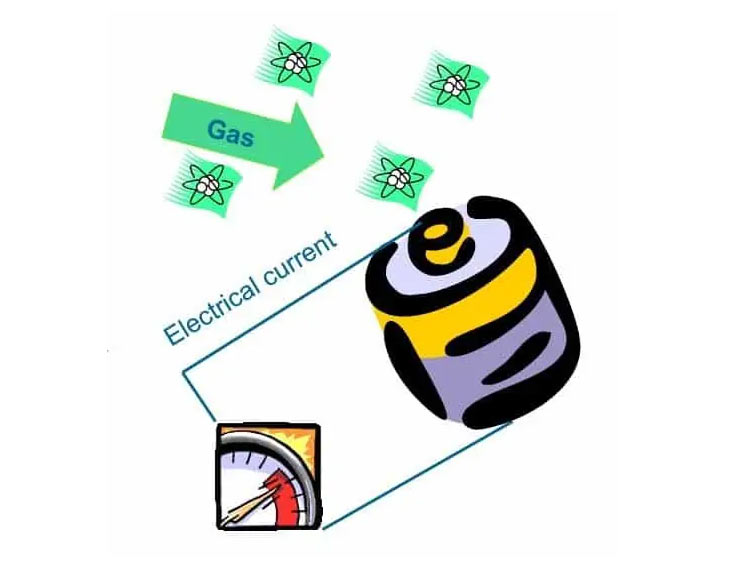
Elektrochemische Sensoren kann man sich als mit Gas betriebene Batterie vorstellen. So lange kein Gas vorhanden ist passiert nichts. So bald ein bestimmtes Gas auf die Arbeitselektrode trifft, findet eine Reaktion statt, bei der Elektronen produziert oder verbraucht werden. Diese fließen über ein hochempfindliches Messgerät zur Gegenelektrode.
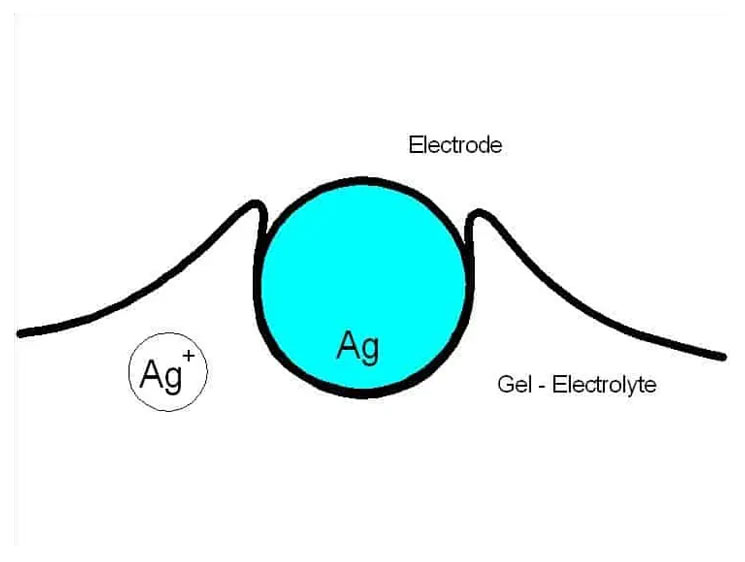
Was passiert nun genau?
In Luft oxidiert das Silber. Man kennt das aus dem Haushalt: Silberbesteck wird an der Luft schwarz. Chemisch gesehen entsteht Silberoxid. Dieses liegt in Form von Ionen vor:
2 Ag0 -> 2 Ag+ + 4 e–
Dieser Prozess läuft so lange, bis sich ein Gleichgewicht aus elementarem Silber und Silberionen eingestellt hat. Nun kommt ein Gas dazu, das mit den Silberionen reagiert: H2S + 2 Ag+ -> Ag2S↓ + 2 H+
Das Silbersulfid ist unlöslich. Damit werden dem Gleichgewicht Ionen entzogen. Die Arbeitselektrode ist gezwungen neue Ionen und damit auch Elektronen zu erzeugen, die durch das Messgerät zur Gegenelektrode fließen. Es fließt ein Strom von einigen nA.
Da jedes Gasmolekül eine ganz bestimmte Anzahl Elektronen erzeugt, ist der Strom direkt proportional zur Anzahl der auftreffenden Gasmoleküle. Nun ist es leicht vorherzusagen, was der oben beschriebene Sensor messen kann: Alle Gase die mit Silber ein unlösliches Salz bilden. Tatsächlich wird diese Sensortechnologie zur Messung von H2S, HCl, HCN und COCl2 verwendet. Dieses Messverfahren ist also sehr spezifisch. Es ist außerdem so empfindlich, dass man damit auch Gase mit sehr niedrigen Grenzwerten zuverlässig messen kann.
Durch die Auswahl der richtigen Elektrodenmaterialien und des richtigen Elektrolyten können gezielt Sensoren entwickelt werden, die ganz bestimmte Stoffe detektieren. Leider sind nicht alle Substanzen reaktiv genug, um ohne Hilfsenergie mit dem zu messenden Gas zu reagieren. Deswegen werden elektrochemische Sensoren hauptsächlich zur Messung anorganischer toxischer Gase und Sauerstoff eingesetzt.
Elektrochemische Sensoren haben einige Vorteile:
Natürlich gibt es auch Nachteile:
3.2 PID Sensoren
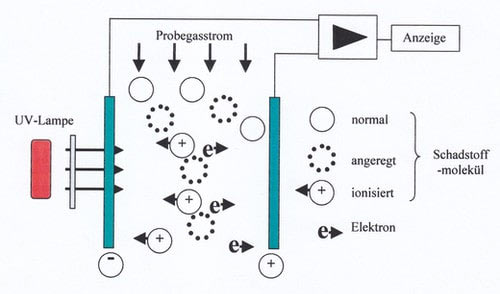
PID Sensoren nutzen die Tatsache, dass sehr energiereiches UV – Licht Gasmoleküle in Radikale aufspaltet. Diese sind elektrisch geladen. Geladene Teilchen kann man leicht zählen, indem man sie durch eine Küvette führt, deren Wandung elektrisch geladen ist. Positiv geladene Teilchen werden von der negativ geladenen Elektrode angezogen und umgekehrt. Dort kompensieren sie ihre elektrische Ladung. Der Entladestrom ist proportional zur Anzahl der Moleküle i. e. der Konzentration.
Als UV – Quellen werden Lampen mit 10,6 oder 11,7 eV verwendet. Diese Energie reicht nicht aus, um Wasser- Sauerstoff- oder Stickstoffmoleküle zu ionisieren. Der PID reagiert also nicht auf Substanzen die ohnehin in Luft vorhanden sind. Dies sind allerdings sehr zahlreiche Substanzen, vor allem viele Kohlenwasserstoffe. Leider werden alle mit unterschiedlicher Empfindlichkeit angezeigt.
Ein PID eignet sich am besten zur Detektion von VOC (Volatile Organic Compounds). Die meisten dieser Substanzen sind Flüssigkeiten. Eine Kalibrierung mit einer Flüssigkeit versucht man wann immer möglich zu vermeiden. Man hat sich daher darauf geeinigt, stets mit Isobuten zu kalibrieren, und die Referenzfaktoren möglichst vieler Stoffe im Vergleich zu Isobuten zu bestimmen. So kann man bequem mit einem Gas kalibrieren. Diese Faktoren findet man in der Literatur, oder z. B. hier zum Download
PID Sensoren haben einige Vorteile:
Natürlich gibt es auch Nachteile:
3.3 Wärmeleitfähigkeitssensoren
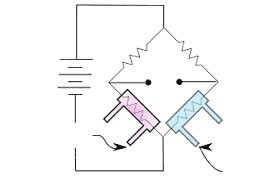
Viele Gase leiten Wärme unterschiedlich gut im Vergleich zu Luft. Diesen Effekt kann man zur Konzentrationsbestimmung verwenden, wenn man die Wärmeleitfähigkeit der Atmosphäre misst.
Dazu bringt man eine Wärmequelle und ein Thermometer in einer durchflossenen Zelle unter. Auch hier verwendet man wieder eine Referenzzelle, um Einflüsse durch Temperatur (hier natürlich extrem wichtig), Feuchte und Druck zu kompensieren.
Enthält nun die Probe in der Messzelle ein Gas, das Wärme besser oder schlechter leitet als Luft, wird das Thermometer der Messzelle einen anderen Wert messen.
Wärmeleitfähigkeitssensoren haben einige Vorteile:
Natürlich gibt es auch Nachteile:

Dr. Josef von Stackelberg
Geschäftsführer COMPUR MONITORS GmbH & Co. KG
Wir beraten Sie gerne
Sie haben Fragen zu unseren Produkten oder wünschen eine unverbindliche Beratung? Wir freuen uns auf Ihre Kontaktaufnahme.